مشخصات فنی Brilliant blue G 250 (C.I. 42655)
| cas number | 6104-58-1 |
| فرمول | C47H48N3O7S2Na |
| بسته بندی | اورجینال کمپانی |
| نام های تجاری | Coomassie® blue G 250 |
| کد محصول | 9598.1 |
| دمای نگهداری | +15 to +25 °C |
ویژگیهای محصول
(0)
0
دیدگاه کاربران
قیمت :
7,392,000
Coomassie brilliant blue نام دو رنگ مشابه تری فنیل متان است که برای استفاده در صنعت نساجی ساخته شده اند اما اکنون معمولاً برای رنگ آمیزی پروتئین ها در بیوشیمی تحلیلی استفاده می شوند. Coomassie brilliant blue G-250 با Coomassie brilliant blue R-250 با افزودن دو گروه متیل متفاوت است. نام "Coomassie" یک علامت تجاری ثبت شده توسط Imperial Chemical Industries است.
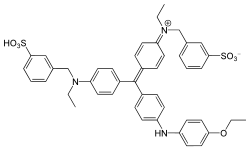

نام Coomassie در پایان قرن نوزدهم به عنوان یک نام تجاری توسط سازنده رنگ مبتنی بر بلکلی، Levinstein Ltd، در بازاریابی طیف وسیعی از رنگهای پشم اسیدی پذیرفته شد. در سال 1896 در خلال جنگ چهارم آنگلو-آشانتی، نیروهای بریتانیایی شهر کوماسی (کوماسی امروزی در غنا) را اشغال کردند. در سال 1918 Levinstein Ltd بخشی از British Dyestuffs شد که در سال 1926 بخشی از Imperial Chemical Industries شد. اگرچه ICI هنوز مالک علامت تجاری Coomassie است، این شرکت دیگر رنگها را تولید نمیکند.
رنگهای آبی دی سولفونه تری فنیل متان اولین بار در سال 1913 توسط ماکس ویلر که در البرفلد آلمان مستقر بود تولید شد. اختراعات مختلفی متعاقباً در مورد سنتز آلی به ثبت رسید.
مقالاتی که در مجلات بیوشیمی منتشر میشوند، اغلب به این رنگها به سادگی با عنوان "Coomassie" اشاره میکنند، بدون اینکه مشخص کنند از کدام رنگ استفاده شده است. در واقع، شاخص رنگ بیش از 40 رنگ را با "Coomassie" در نام آنها فهرست می کند. رنگهای دیگر Coomassie "آبی" نیز وجود دارد. به عنوان مثال، فهرست Merck (ویرایش دهم) Coomassie Blue RL (Acid Blue 92, C.I. 13390) را فهرست می کند که ساختار کاملاً متفاوتی دارد.
پسوند "R" در نام Coomassie brilliant blue R-250 مخفف "قرمز" است زیرا رنگ آبی رنگ دارای رنگ قرمز کمی است. برای نوع "G" رنگ آبی رنگ مایل به سبز بیشتری دارد. "250" در اصل نشان دهنده خلوص رنگ است.
رنگ این دو رنگ به اسیدیته محلول بستگی دارد. شکل «G» رنگ به تفصیل بررسی شده است. در pH کمتر از 0 رنگ دارای رنگ قرمز با حداکثر جذب در طول موج 465 نانومتر است. در pH حدود 1 رنگ سبز با حداکثر جذب در 620 نانومتر است در حالی که بالاتر از pH 2 رنگ آبی روشن با حداکثر 595 نانومتر است. در pH 7 رنگ دارای ضریب انقراض 43000 M-1cm-1 است.
رنگ های مختلف نتیجه حالت های باردار مختلف مولکول رنگ هستند. در شکل قرمز، هر سه اتم نیتروژن حامل بار مثبت هستند. دو گروه اسید سولفونیک pKa بسیار پایینی دارند و معمولاً دارای بار منفی خواهند بود، بنابراین در pH حدود صفر رنگ یک کاتیون با بار کلی +1 خواهد بود. رنگ سبز مربوط به شکلی از رنگ بدون شارژ کلی است. در محیط های خنثی (pH 7)، فقط اتم نیتروژن قسمت دی فنیل آمین حامل بار مثبت است و مولکول رنگ آبی یک آنیون با بار کلی 1- است. مقادیر pKa برای تلفات دو پروتون به ترتیب 1.15 و 1.82 است. پروتون نهایی در شرایط قلیایی از بین می رود و رنگ صورتی می شود (pKa 12.4).
این رنگ به صورت الکترواستاتیک اما غیرکووالانسی با گروه های آمینو و کربوکسیل پروتئین ها برهمکنش دارد. مولکول های رنگ به پروتئین ها، از جمله پروتئین های موجود در پشم (کراتین) متصل می شوند تا یک کمپلکس پروتئین-رنگ تشکیل دهند. تشکیل کمپلکس شکل آنیونی رنگ با بار منفی را تثبیت می کند و رنگ آبی را تولید می کند، حتی در شرایط اسیدی که اکثر مولکول های موجود در محلول به شکل کاتیونی هستند. این اساس سنجش برادفورد است که پروتئین را با اتصال رنگ آبی درخشان Coomassie تعیین می کند. اتصال رنگ به پروتئین باعث تغییر در حداکثر جذب رنگ از 465 به 595 نانومتر می شود. افزایش جذب در طول موج 595 نانومتر برای تعیین غلظت پروتئین بررسی می شود.
رنگ همچنین با ماده شوینده آنیونی سدیم دودسیل سولفات (SDS) یک کمپلکس تشکیل می دهد. تشکیل این کمپلکس حالت خنثی و سبز رنگ را تثبیت می کند. این اثر می تواند با تخمین غلظت پروتئین با استفاده از روش برادفورد تداخل داشته باشد. همچنین این احتمال وجود دارد که شوینده آنیونی با رنگ برای اتصال به پروتئین رقابت کند.


Coomassie brilliant blue G در محلول ایزوپروپانول Coomassie brilliant blue G جامد
Coomassie brilliant blue R-250 برای اولین بار در سال 1963 توسط Fazekas de St. Groth و همکارانش برای تجسم پروتئین ها استفاده شد. نمونه های پروتئینی به روش الکتروفورزی روی ورقه استات سلولز جدا شدند. سپس ورق در اسید سولفوسالیسیلیک خیس شد تا نوارهای پروتئینی ثابت شود و به محلول رنگ منتقل شود.
دو سال بعد در سال 1965 مایر و لامبرت از Coomassie برلیانت آبی R-250 برای رنگ آمیزی نمونه های پروتئینی پس از جداسازی الکتروفورتیک در ژل پلی آکریل آمید استفاده کردند. آنها ژل را در محلول رنگی حاوی متانول، اسید استیک و آب خیس کردند. همانطور که رنگ، ژل پلی آکریل آمید و همچنین پروتئین را رنگ می کرد، به منظور تجسم نوارهای پروتئینی مورد نیاز برای رنگ آمیزی ژل، که آنها به صورت الکتروفورزی انجام دادند. انتشارات بعدی گزارش کردند که ژل های پلی آکریل آمید را می توان با موفقیت با استفاده از محلول اسید استیک رنگ آمیزی کرد.
اولین گزارش استفاده از فرم G رنگ برای تجسم نوارهای پروتئینی در ژل های پلی آکریل آمید در سال 1967 منتشر شد، جایی که رنگ در محلول اسید استیک حاوی متانول حل شد. متعاقباً کشف شد که باندهای پروتئینی را می توان بدون رنگ آمیزی پلی آکریل آمید با استفاده از کلوئیدی از فرم G رنگ در محلول اسید تری کلرواستیک بدون متانول رنگ آمیزی کرد. با این روش دیگر نیازی به رنگ آمیزی ژل نبود. فرمولهای مدرن معمولاً از کلوئیدی از رنگ G در محلولی حاوی اسید فسفریک، اتانول (یا متانول) و سولفات آمونیوم (یا سولفات آلومینیوم) استفاده میکنند.
روش برادفورد از خواص طیفی Coomassie brilliant blue G-250 برای تخمین مقدار پروتئین در محلول استفاده می کند. یک نمونه پروتئین به محلول رنگ در اسید فسفریک و اتانول اضافه می شود. در شرایط اسیدی، رنگ معمولاً قهوهای است، اما با اتصال به پروتئین، شکل آبی رنگ تولید میشود. جذب نوری محلول در طول موج 595 نانومتر اندازه گیری می شود. رنگ به دلیل سطح بالایی از حساسیت آن مورد توجه قرار گرفته است: 5 میکروگرم پروتئین [شفاف سازی مورد نیاز] قابل تشخیص است. با این حال، از جمله معایب این روش، تغییر رنگ آن با پروتئین های مختلف است: تغییر جذب در واحد جرم پروتئین با نوع پروتئین متفاوت است.
در اتصال به پروتئین، مولکول رنگ آبی درخشان G-250 کوماسی با بار منفی، بار منفی کلی به پروتئین می دهد. این ویژگی را می توان برای جداسازی پروتئین ها یا کمپلکس های پروتئینی با استفاده از الکتروفورز ژل پلی آکریل آمید در شرایط غیر دناتوره کننده در تکنیکی به نام PAGE بومی آبی استفاده کرد. تحرک کمپلکس در ژل پلی آکریل آمید هم به اندازه کمپلکس پروتئین (به عنوان مثال وزن مولکولی) و هم به مقدار رنگ متصل به پروتئین بستگی دارد.
رنگ آمیزی آبی کوماسی همچنین می تواند به عنوان یک روش رنگ آمیزی کنترل بارگذاری در آنالیز وسترن بلات استفاده شود. این به عنوان یک لکه پیش آنتی بادی آنیونی استفاده می شود.
در سال 2009، آبی درخشان G در آزمایشهای علمی برای درمان آسیبهای ستون فقرات در موشهای آزمایشگاهی استفاده شد. این دارو با کاهش واکنش تورم طبیعی بدن عمل میکند که میتواند باعث مرگ نورونهای ناحیه بر اثر استرس متابولیک شود. آزمایش بر روی موشها مؤثر بود. در مقایسه با موشهایی که رنگ دریافت نکرده بودند، موشهایی که تحت درمان با رنگ قرار گرفتند در تستهای حرکتی بهتر عمل کردند. مشخص نیست که آیا این درمان می تواند به طور موثر در انسان استفاده شود یا خیر. آزمایشهای حیوانی رنگ را ظرف 15 دقیقه پس از آسیب تزریق کردند، اما برای مؤثر بودن در شرایط واقعی، جایی که ممکن است برای رسیدن بیمار به اورژانس زمان لازم باشد، درمان باید حتی زمانی که تا دو ساعت انجام میشود مؤثر باشد. بعد از آسیب دیدگی تنها عارضه جانبی گزارش شده این بود که موش ها به طور موقت آبی شدند.
تحت نامهای تجاری ILM Blue و Brilliant Peel، آبی درخشان G به عنوان لکه برای کمک به جراحان در جراحی شبکیه استفاده میشود. در دسامبر 2019، آبی درخشان G (با نام تجاری TissueBlue، DORC International، هلند) برای استفاده در انسان در ایالات متحده تایید شد.
Tissueblue در ژانویه 2021 برای استفاده پزشکی در کانادا تایید شد.
توانایی رنگ Coomassie در هدف قرار دادن اسیدهای آمینه با گروه های معطر (فنیل آلانین، تیروزین، تریپتوفان) و زنجیره های جانبی پایه (لیزین، آرژنین و هیستیدین) اجازه می دهد تا از روش برادفورد برای تجزیه و تحلیل اثر انگشت استفاده شود. این روش با موفقیت برای شناسایی جنسیت بیولوژیکی اثر انگشت مورد استفاده قرار گرفت. نشان داده شد که نمونههای ماده در طول موجهای مشابه، جذب بالاتری نسبت به نمونههای مرد دارند. این روش سادهتری را برای آنالیز اثر انگشت با کاهش تعداد آمینو اسیدهای مورد نیاز برای آنالیز از 23 به 6 فراهم میکند و نیاز به آمادهسازی کمی یا بدون نیاز به سنجش دارد، برخلاف روش شیمیایی نین هیدرین، که به آمادهسازی سنجش مانند گرمایش و آبشار آنزیمی نیاز دارد.
| cas number | 6104-58-1 |
| فرمول | C47H48N3O7S2Na |
| بسته بندی | اورجینال کمپانی |
| نام های تجاری | Coomassie® blue G 250 |
| کد محصول | 9598.1 |
| دمای نگهداری | +15 to +25 °C |


فروشگاه انلاین مارکت چمی توسط شرکت کیمیاگستر پویش با پشتوانه 20سال سابقه درخشان در امر واردات و فروش و توزیع موادشیمیایی آزمایشگاهی،صنعتی و مواد اولیه دارویی و با اتکا به موجودی بیش از 1000عنوان کالای شیمیایی در انبار مجموعه، با هدف تسهیل خدمت رسانی به پزوهشگران فرهیخته کشور عزیزمان ایران راه اندازی گردید.در این فروشگاه سعی کردیم به دغدغه های بحق مصرف کنندگان محصولات شیمیایی راهکارهای مناسب ارائه دهیم.


