مشخصات فنی Sodium carbonate anhydrous
| فرمول | Na2CO3 |
| بسته بندی | اورجینال کمپانی |
| نام های تجاری | Anhydrous soda |
| تاریخ انقضاء | 2021/8 تاریخ گذشته فروش به شرط تست محصول |
| کد محصول | SO01151000 |
| cas number | 497-19-8 |
ویژگیهای محصول
(0)
0
دیدگاه کاربران
قیمت :
کربنات سدیم (همچنین به نامهای سودا شستشو، خاکستر سودا و کریستالهای سودا نیز شناخته میشود) یک ترکیب معدنی با فرمول Na2CO3 و هیدراتهای مختلف آن است. همه شکل ها نمک های سفید، بی بو و محلول در آب هستند که محلول های قلیایی در آب تولید می کنند. از نظر تاریخی، آن را از خاکستر گیاهانی که در خاکهای غنی از سدیم رشد میکردند استخراج میکردند، و از آنجا که خاکستر این گیاهان غنی از سدیم با خاکستر چوب (که زمانی برای تولید پتاس استفاده میشد) تفاوت قابلتوجهی داشت، کربنات سدیم به نام «خاکستر سودا» معروف شد. ". این ماده در مقادیر زیادی از کلرید سدیم و سنگ آهک توسط فرآیند Solvay و همچنین با کربناته کردن هیدروکسید سدیم که با استفاده از فرآیند کلر-قلیایی ساخته می شود، تولید می شود.
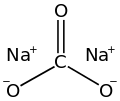
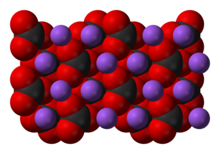
هیدراته ها
کربنات سدیم به صورت سه هیدرات و نمک بی آب به دست می آید:
سدیم کربنات دکاهیدرات (ناترون)، Na2CO3·10H2O، که به راحتی شکوفا می شود و مونوهیدرات را تشکیل می دهد.
هپتا هیدرات کربنات سدیم (به شکل معدنی شناخته نشده)، Na2CO3·7H2O.
کربنات سدیم مونوهیدرات (ترموناتریت)، Na2CO3·H2O. همچنین به عنوان کربنات کریستال شناخته می شود.
کربنات سدیم بی آب (ناتریت)، که به عنوان سودای کلسینه نیز شناخته می شود، از گرم کردن هیدرات ها تشکیل می شود. همچنین هنگامی که هیدروژن کربنات سدیم گرم می شود (کلسینه می شود) تشکیل می شود. در مرحله نهایی فرآیند Solvay.
دکاهیدرات از محلول های آب متبلور در محدوده دمایی -2.1 تا +32.0 درجه سانتی گراد، هپتا هیدرات در محدوده باریک 32.0 تا 35.4 درجه سانتی گراد و بالاتر از این دما مونوهیدرات تشکیل می شود. در هوای خشک، دکاهیدرات و هپتا هیدرات آب خود را از دست می دهند و مونوهیدرات می دهند. هیدرات های دیگری گزارش شده است، به عنوان مثال. با 2.5 واحد آب در هر واحد کربنات سدیم ("همی هیدرات پنتا").
سدیم کربنات دکاهیدرات (Na2CO3·10H2O)، همچنین به عنوان سودای شستشو شناخته می شود، رایج ترین هیدرات کربنات سدیم است که حاوی 10 مولکول آب متبلور است. خاکستر سودا در آب حل می شود و برای بدست آوردن سودا متبلور می شود.
این یکی از معدود کربنات های فلزی است که در آب محلول است.
برخی از کاربردهای رایج کربنات سدیم عبارتند از:
به عنوان یک عامل پاک کننده برای مصارف خانگی مانند شستن لباس ها. کربنات سدیم جزء بسیاری از پودرهای صابون خشک است. از طریق فرآیند صابونی شدن، که چربی ها و گریس ها را به نمک های محلول در آب (به ویژه صابون ها) تبدیل می کند، خاصیت شوینده دارد.
برای کاهش سختی آب استفاده می شود (نگاه کنید به § نرم شدن آب).
از آن در ساخت شیشه، صابون و کاغذ استفاده می شود (به بخش تولید شیشه مراجعه کنید).
در ساخت ترکیبات سدیم مانند بوراکس استفاده می شود.
کربنات سدیم به عنوان یک شار برای سیلیس (SiO2، نقطه ذوب 1713 درجه سانتی گراد) عمل می کند و نقطه ذوب مخلوط را به چیزی می رساند که بدون مواد خاص قابل دستیابی است. این "لیوان سودا" به آرامی محلول در آب است، بنابراین مقداری کربنات کلسیم به مخلوط مذاب اضافه می شود تا شیشه نامحلول شود. شیشه بطری و پنجره ("شیشه سودا-آهک" با دمای انتقال ~570 درجه سانتیگراد) از ذوب چنین مخلوط هایی از کربنات سدیم، کربنات کلسیم و ماسه سیلیس (دی اکسید سیلیکون (SiO2)) ساخته می شود. هنگامی که این مواد گرم می شوند، کربنات ها دی اکسید کربن آزاد می کنند. به این ترتیب کربنات سدیم منبع اکسید سدیم است. شیشه سودا-آهک برای قرن ها رایج ترین شکل شیشه بوده است. همچنین یک ورودی کلیدی برای تولید شیشه ظروف غذاخوری است.
آب سخت معمولا حاوی یون های کلسیم یا منیزیم است. کربنات سدیم برای حذف این یون ها و جایگزینی آنها با یون های سدیم استفاده می شود.
کربنات سدیم منبع کربنات محلول در آب است. یونهای کلسیم و منیزیم پس از درمان با یونهای کربنات، رسوبات جامد نامحلول را تشکیل میدهند:
Ca2+ + CO2−3 → CaCO3 (s)
آب نرم می شود زیرا دیگر حاوی یون های کلسیم و یون منیزیم محلول نیست.
کربنات سدیم کاربردهای مختلفی در آشپزی دارد، عمدتاً به این دلیل که پایه قویتری نسبت به جوش شیرین (بی کربنات سدیم) اما ضعیفتر از لیمو است (که ممکن است به هیدروکسید سدیم یا کمتر متداول به هیدروکسید پتاسیم اشاره داشته باشد). قلیاییت بر تولید گلوتن در خمیرهای ورز داده شده تأثیر می گذارد و همچنین با کاهش دمایی که واکنش Maillard در آن رخ می دهد، قهوه ای شدن را بهبود می بخشد. بنابراین برای استفاده از اثر قبلی، کربنات سدیم یکی از اجزای کانسوی (かん水) است، محلولی از نمک های قلیایی که برای دادن طعم خاص و بافت جویدنی به رشته فرنگی رامن ژاپنی استفاده می شود. محلول مشابهی در غذاهای چینی برای تهیه لامیان به دلایل مشابه استفاده می شود. نانوایان کانتونی به طور مشابه از کربنات سدیم به عنوان جایگزینی برای آب شیرین استفاده می کنند تا به کیک های ماه بافت خاص خود را بدهد و قهوه ای شدن را بهبود بخشد. در آشپزی آلمانی (و غذاهای اروپای مرکزی به طور گستردهتر)، نانهایی مانند چوب شور و لیمو رولهایی که بهطور سنتی با لیمو برای بهبود قهوهای شدن استفاده میشوند، میتوانند به جای آن با کربنات سدیم درمان شوند. کربنات سدیم به اندازه لیمو قهوه ای قوی ایجاد نمی کند، اما کار با آن بسیار ایمن تر و آسان تر است.
از کربنات سدیم در تولید پودر شربت استفاده می شود. احساس سرد شدن و وز کردن ناشی از واکنش گرماگیر بین کربنات سدیم و اسید ضعیف، معمولاً اسید سیتریک است که گاز دی اکسید کربن آزاد می کند، که زمانی رخ می دهد که شربت توسط بزاق مرطوب شود.
کربنات سدیم همچنین در صنایع غذایی به عنوان یک افزودنی غذایی (E500) به عنوان تنظیم کننده اسیدیته، عامل ضد انعقاد، عامل افزایش دهنده و تثبیت کننده استفاده می شود. همچنین در تولید snus برای تثبیت PH محصول نهایی استفاده می شود.
در حالی که احتمال کمتری ایجاد سوختگی شیمیایی نسبت به لیمو وجود دارد، اما باید هنگام کار با کربنات سدیم در آشپزخانه احتیاط کرد، زیرا برای ظروف، ظروف و فویل آلومینیومی خورنده است.
کربنات سدیم نیز به عنوان یک پایه نسبتا قوی در زمینه های مختلف استفاده می شود. به عنوان یک قلیایی معمولی، در بسیاری از فرآیندهای شیمیایی ترجیح داده می شود، زیرا ارزان تر از هیدروکسید سدیم است و حمل و نقل آن بسیار ایمن تر است. ملایم بودن آن به ویژه استفاده از آن را در مصارف خانگی توصیه می کند.
به عنوان مثال، از آن به عنوان یک تنظیم کننده pH برای حفظ شرایط قلیایی پایدار لازم برای عملکرد اکثر عوامل تولید فیلم عکاسی استفاده می شود. همچنین یک افزودنی رایج در استخرهای شنا و آب آکواریوم برای حفظ pH مطلوب و سختی کربناته (KH) است. در رنگرزی با رنگهای واکنشگر فیبر، کربنات سدیم (اغلب با نامی مانند تثبیتکننده خاکستر سودا یا فعالکننده خاکستر سودا) برای اطمینان از پیوند شیمیایی مناسب رنگ با الیاف سلولزی (گیاهی)، معمولاً قبل از رنگآمیزی (برای رنگهای کراواتی) استفاده میشود. مخلوط با رنگ (برای رنگ آمیزی)، یا پس از رنگرزی (برای رنگرزی غوطه وری). همچنین در فرآیند فلوتاسیون کف برای حفظ pH مطلوب به عنوان یک نرم کننده شناور علاوه بر CaO و سایر ترکیبات با پایه ملایم استفاده می شود.
بی کربنات سدیم (NaHCO3) یا جوش شیرین، همچنین جزء کپسول های آتش نشانی، اغلب از کربنات سدیم تولید می شود. اگرچه NaHCO3 خود محصول واسطه ای از فرآیند Solvay است، گرمایش مورد نیاز برای حذف آمونیاکی که آن را آلوده می کند، مقداری NaHCO3 را تجزیه می کند و واکنش Na2CO3 نهایی با CO2 را مقرون به صرفه تر می کند:
Na2CO3 + CO2 + H2O → 2NaHCO3
در یک واکنش مرتبط، از کربنات سدیم برای ساخت بی سولفیت سدیم (NaHSO3) استفاده می شود که برای روش "سولفیت" جداسازی لیگنین از سلولز استفاده می شود. این واکنش برای حذف دی اکسید گوگرد از گازهای دودکش در نیروگاه ها مورد استفاده قرار می گیرد:
Na2CO3 + SO2 + H2O → NaHCO3 + NaHSO3
این برنامه رایج تر شده است، به ویژه در جایی که ایستگاه ها باید کنترل های انتشار دقیق را رعایت کنند.
کربنات سدیم توسط صنعت پنبه برای خنثی کردن اسید سولفوریک مورد نیاز برای جداسازی اسید پنبه دانه های فازی استفاده می شود.
همچنین برای تشکیل کربناتهای فلزات دیگر از طریق تبادل یونی، اغلب با سولفاتهای فلزات دیگر، استفاده میشود.
کربنات سدیم توسط صنعت آجر به عنوان یک عامل مرطوب کننده برای کاهش مقدار آب مورد نیاز برای اکسترود کردن خاک رس استفاده می شود. در ریخته گری به آن "عامل پیوند" می گویند و برای چسبیدن آلژینات مرطوب به آلژینات ژل شده استفاده می شود. کربنات سدیم در خمیردندان ها استفاده می شود، جایی که به عنوان عامل کف کننده و ساینده عمل می کند و به طور موقت PH دهان را افزایش می دهد.
کربنات سدیم همچنین در فرآوری و دباغی پوست حیوانات استفاده می شود.
| فرمول | Na2CO3 |
| بسته بندی | اورجینال کمپانی |
| نام های تجاری | Anhydrous soda |
| تاریخ انقضاء | 2021/8 تاریخ گذشته فروش به شرط تست محصول |
| کد محصول | SO01151000 |
| cas number | 497-19-8 |


فروشگاه انلاین مارکت چمی توسط شرکت کیمیاگستر پویش با پشتوانه 20سال سابقه درخشان در امر واردات و فروش و توزیع موادشیمیایی آزمایشگاهی،صنعتی و مواد اولیه دارویی و با اتکا به موجودی بیش از 1000عنوان کالای شیمیایی در انبار مجموعه، با هدف تسهیل خدمت رسانی به پزوهشگران فرهیخته کشور عزیزمان ایران راه اندازی گردید.در این فروشگاه سعی کردیم به دغدغه های بحق مصرف کنندگان محصولات شیمیایی راهکارهای مناسب ارائه دهیم.


