اتیلن دی آمین تتراستیک اسید چیست؟
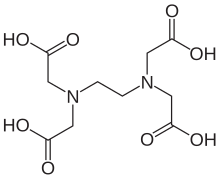
اتیلن دی آمین تتراستیک اسید (EDTA) که پس از مخفف خود اسید EDTA نیز نامیده می شود، یک اسید آمینه پلی کربوکسیلیک با فرمول [CH2N(CH2CO2H)2]2 است. این جامد سفید رنگ و نامحلول در آب به طور گسترده برای اتصال به آهن (Fe2+/Fe3+) و یونهای کلسیم (Ca2+) استفاده میشود و کمپلکسهای محلول در آب را حتی در pH خنثی تشکیل میدهد. بنابراین برای حل کردن مقیاس حاوی آهن و کلسیم و همچنین برای تحویل یون های آهن در شرایطی که اکسیدهای آن نامحلول هستند استفاده می شود. EDTA به صورت چند نمک در دسترس است، به ویژه دی سدیم EDTA، سدیم کلسیم ادتات و تترا سدیم EDTA، اما همه اینها عملکرد مشابهی دارند.
از ادتا استفاده می کنند در
منسوجات و کاغذ
در صنعت، EDTA عمدتاً برای جداسازی (پیوند یا محدود کردن) یونهای فلزی در محلول آبی استفاده میشود. در صنعت نساجی از ناخالصی های یون فلزی از تغییر رنگ محصولات رنگ شده جلوگیری می کند. در صنعت خمیر و کاغذ، EDTA از توانایی یون های فلزی، به ویژه Mn2+، از کاتالیزور نامتناسب پراکسید هیدروژن، که در سفید کردن بدون کلر استفاده می شود، جلوگیری می کند.
غذا
به روشی مشابه، EDTA به عنوان نگهدارنده یا تثبیت کننده به برخی مواد غذایی اضافه می شود تا از تغییر رنگ اکسیداتیو کاتالیزوری که توسط یون های فلزی کاتالیز می شود، جلوگیری شود.
نرم کننده آب
کاهش سختی آب در کاربردهای لباسشویی و انحلال رسوب در دیگها هر دو به EDTA و کمپلکسهای مرتبط برای اتصال Ca2+، Mg2+ و همچنین سایر یونهای فلزی وابسته است. پس از اتصال به EDTA، این کمپلکسهای فلزی کمتر احتمال دارد که رسوب تشکیل دهند یا با عملکرد صابونها و مواد شوینده تداخل کنند. به دلایل مشابه، محلولهای تمیزکننده اغلب حاوی EDTA هستند. به روشی مشابه از EDTA در صنعت سیمان برای تعیین آهک آزاد و منیزیم آزاد در سیمان و کلینکر استفاده می شود.
انحلال یون های Fe3+ در pH خنثی یا کمتر از آن را می توان با استفاده از EDTA انجام داد. این خاصیت در کشاورزی از جمله هیدروپونیک مفید است. با این حال، با توجه به وابستگی به pH تشکیل لیگاند، EDTA برای بهبود حلالیت آهن در خاکهای خنثی بالا مفید نیست. در غیر این صورت، در PH نزدیک به خنثی و بالاتر، آهن (III) نمکهای نامحلول تشکیل میدهد که کمتر در دسترس گونههای گیاهی حساس هستند.
اسکراب کردن
آبی [Fe(EDTA)]- برای حذف سولفید هیدروژن از جریان گاز استفاده می شود. این تبدیل با اکسید کردن سولفید هیدروژن به گوگرد عنصری که غیرفرار است به دست میآید:
2 [Fe(EDTA)]− + H2S → 2 [Fe(EDTA)]2− + S + 2 H+
در این کاربرد، مرکز آهن (III) به مشتق آهن (II) خود کاهش می یابد، که سپس می تواند توسط هوا دوباره اکسید شود. به روشی مشابه، اکسیدهای نیتروژن از جریان گاز با استفاده از [Fe(EDTA)] 2- حذف می شوند.
خواص اکسید کننده [Fe(EDTA)]- نیز در عکاسی مورد استفاده قرار می گیرد، جایی که از آن برای حل کردن ذرات نقره استفاده می شود.
کروماتوگرافی تبادل یونی
EDTA در جداسازی فلزات لانتانید با کروماتوگرافی تبادل یونی استفاده شد. کامل شده توسط F. H. Spedding و همکاران. در سال 1954، این روش بر افزایش ثابت پایداری کمپلکسهای لانتانید EDTA با عدد اتمی تکیه داشت. با استفاده از دانه های پلی استایرن سولفونه شده و Cu2+ به عنوان یون نگهدارنده، EDTA باعث می شود لانتانیدها به پایین ستون رزین مهاجرت کنند و در عین حال به نوارهایی از لانتانیدهای خالص جدا شوند. لانتانیدها به ترتیب کاهش عدد اتمی شسته می شوند. با توجه به هزینه های این روش، نسبت به استخراج با حلال مخالف، تبادل یونی اکنون فقط برای به دست آوردن بالاترین خلوص لانتانیدها (معمولاً بیشتر از 99.99٪) استفاده می شود.
دارو
سدیم کلسیم ادتات، یک مشتق EDTA، برای اتصال یونهای فلزی در عمل کیلاسیون درمانی، مانند درمان مسمومیت با جیوه و سرب، استفاده میشود. به روشی مشابه برای حذف آهن اضافی از بدن استفاده می شود. این درمان برای درمان عوارض ناشی از تزریق مکرر خون، همانطور که برای درمان تالاسمی استفاده می شود، استفاده می شود.
دندانپزشکی
دندانپزشکان و اندودنتیست ها از محلول های EDTA برای حذف مواد معدنی (لایه اسمیر) و روانکاری کانال های ریشه در درمان ریشه استفاده می کنند. این روش به آماده سازی کانال های ریشه برای انسداد کمک می کند. علاوه بر این، محلولهای EDTA با افزودن یک سورفکتانت، کلسیفیکاسیونهای داخل کانال ریشه را شل میکند و امکان ابزارسازی (شکلدهی کانال) را فراهم میکند و پیشرفت آپیکالی فایل را در کانال ریشه محکم یا کلسیفیه به سمت راس تسهیل میکند.
قطره چشم
این ماده به عنوان یک نگهدارنده (معمولاً برای تقویت عملکرد نگهدارنده دیگری مانند کلرید بنزالکونیوم یا تیومرسال) در آماده سازی های چشمی و قطره ها عمل می کند.
تحلیل و بررسی
در تستهای تشخیص پزشکی و عملکرد اعضای بدن (در اینجا، تست عملکرد کلیه)، کمپلکس کروم (III) [Cr(EDTA)]- (به عنوان کروم-51 رادیواکتیو (51Cr)) به صورت داخل وریدی تجویز میشود و فیلتراسیون آن در ادرار کنترل میشود. این روش برای ارزیابی میزان فیلتراسیون گلومرولی (GFR) در پزشکی هسته ای مفید است.
EDTA به طور گسترده در تجزیه و تحلیل خون استفاده می شود. این یک ضد انعقاد برای نمونههای خون برای CBC/FBC است، جایی که EDTA کلسیم موجود در نمونه خون را کیل میکند، روند انعقاد را متوقف میکند و مورفولوژی سلولهای خونی را حفظ میکند. لوله های حاوی EDTA با رویه های اسطوخودوس (بنفش) یا صورتی مشخص شده اند. EDTA همچنین در لولههای قهوهای مایل به زرد برای آزمایش سرب است و میتواند در لولههای رویال آبی برای آزمایش فلزات مورد استفاده قرار گیرد.
EDTA یک پخش کننده لجن است و مشخص شده است که در کاهش رشد باکتری ها در طول کاشت لنزهای داخل چشمی (IOLs) بسیار موثر است.
طب جایگزین
برخی از پزشکان جایگزین بر این باورند که EDTA به عنوان یک آنتی اکسیدان عمل می کند و از آسیب رساندن رادیکال های آزاد به دیواره رگ های خونی جلوگیری می کند و در نتیجه آترواسکلروز را کاهش می دهد. این ایده ها توسط مطالعات علمی پشتیبانی نمی شوند و به نظر می رسد با برخی از اصول پذیرفته شده در حال حاضر در تضاد هستند. FDA ایالات متحده آن را برای درمان آترواسکلروز تایید نکرده است.
لوازم آرایشی
در شامپوها، پاککنندهها و سایر محصولات مراقبت شخصی، نمکهای EDTA بهعنوان عامل جداکننده برای بهبود پایداری آنها در هوا استفاده میشوند.
کاربردهای آزمایشگاهی
در آزمایشگاه، EDTA به طور گسترده برای مهار یونهای فلزی استفاده میشود: در بیوشیمی و زیستشناسی مولکولی، تخلیه یون معمولاً برای غیرفعال کردن آنزیمهای وابسته به فلز، یا به عنوان سنجشی برای واکنشپذیری آنها یا برای سرکوب آسیب به DNA، پروتئینها و پلیساکاریدها استفاده میشود. EDTA همچنین به عنوان یک بازدارنده انتخابی در برابر آنزیم های هیدرولیزکننده dNTP (Taq polymerase، dUTPase، MutT)، آرژیناز کبدی و پراکسیداز ترب کوهی مستقل از کیلاسیون یون فلزی عمل می کند. این یافته ها بازاندیشی در مورد استفاده از EDTA به عنوان یک جاذب یون فلزی غیرفعال بیوشیمیایی در آزمایشات آنزیمی را ترغیب می کند. در شیمی تجزیه، EDTA در تیتراسیون های کمپلکس سنجی و تجزیه و تحلیل سختی آب یا به عنوان یک عامل پوشش دهنده برای جداسازی یون های فلزی که در تجزیه و تحلیل ها تداخل دارند، استفاده می شود.
EDTA کاربردهای تخصصی زیادی در آزمایشگاههای زیست پزشکی پیدا میکند، مانند چشم پزشکی دامپزشکی به عنوان یک آنتیکلاژناز برای جلوگیری از بدتر شدن زخم قرنیه در حیوانات. در کشت بافت، EDTA به عنوان یک عامل کیلیت کننده استفاده می شود که به کلسیم متصل می شود و از اتصال کادرین ها بین سلول ها جلوگیری می کند، از تجمع سلول های رشد یافته در سوسپانسیون مایع یا جدا شدن سلول های چسبنده برای عبور جلوگیری می کند. در هیستوپاتولوژی، EDTA را می توان به عنوان یک عامل کلسیم زدا استفاده کرد که امکان برش بخش ها را با استفاده از میکروتوم پس از دمینرالیزه شدن نمونه بافت فراهم می کند.






























